「新薬申請サービス」は、医薬品の製造販売承認申請から取得までに必要な資料作成をワンストップで支援するアウトソーシングサービスです。
当社はこれまでに100社以上の製薬会社にサービスを提供し、20年以上にわたる長年の経験と高い専門性で業界のリーディングカンパニーとして高いシェアを獲得しています。
富士フイルムシステムサービスは、「新薬申請サービス」を通じて製薬会社の医薬品製造・販売承認申請を支援することにより、新薬を一日でも早く患者様に届けられるよう貢献していきます。
お客様の申請戦略や経営環境に応じて、最適なサービスを組み合わせて、ワンストップでご支援いたします。
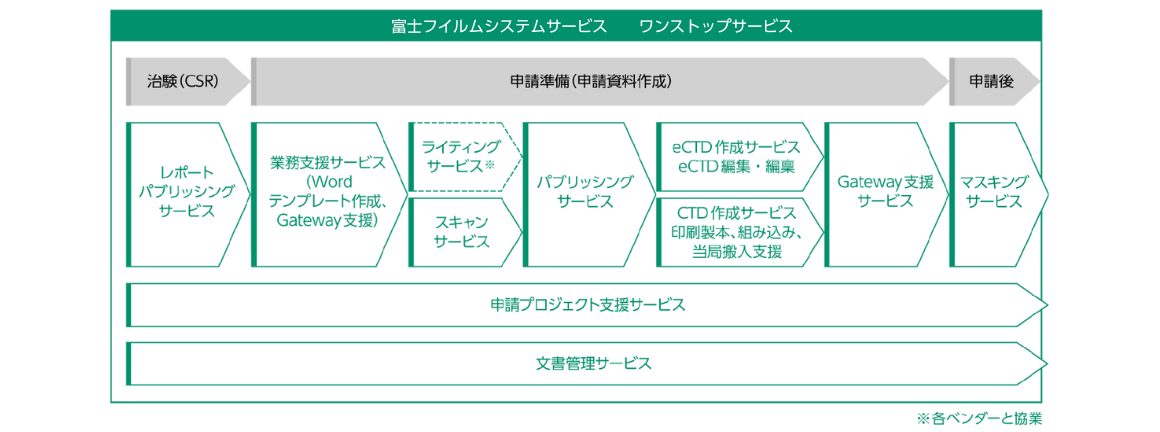
日本では2022年4月より、eCTD v4.0に対応した資料による申請の受付が開始され、2026年4月から同規制への対応が義務化される予定です。
当社では、従来規制のeCTD v3.2.2と同様に、eCTD v4.0においてもワンストップで支援するサービスおよびeCTD v4.0の対応準備に向けたコンサルティングサービスを提供しております。
- eCTD v4.0対応導入準備サポート
- フォルダ作成、文書間リンク作成、リネーム、XMLインスタンス作成、バリデータ検証
- 当局提出eCTD v4.0のビューア環境の提供(eCTD v4.0最終確認時)
CTD/eCTD 新薬承認申請資料作成支援サービスに関する資料をご用意しました。
下部お問い合わせボタンより資料ダウンロードご希望のサービス名を記載のうえお申し込みください。
累計117社・650品目以上の申請支援サービスを過去20年にわたり提供させていただいております。
また、多くのお客様にリピートオーダーをいただき、年間100件程度の申請、審査に対応させていただいております。

※2022年9月現在
eCTD導入の初期段階よりサービスを提供し、またさまざまな申請資料の作成・提出をサポートしてまいりました。
これら経験に基づいた運用手順・仕様の最適化を行うことにより、納品物の品質を高く保つことを可能としております。

申請の頻度が少なく社内体制整備が難しいお客様や、コンスタントに申請は行うが、たまたま申請が集中してしまったお客様など、お客様要望に合わせて最適なサービスの提供を行うことが可能です。
これにより、環境を社内で保持した場合と比べ、運用管理コストを大幅に削減することを可能とします。