22年に渡りご支援してきた、医薬品の製造販売承認申請から取得までに必要な資料作成をワンストップでご支援してきた「新薬申請サービス」のノウハウを生かしたサービスです。具体的には、申請資料作成の上流工程である試験総括報告書(CSR)の作成段階で規制要件仕様で申請添付資料を作成するサービスで、新薬の製造販売申請の納期短縮に繋がります。お客様はコア業務である申請資料のコンテンツ作成(執筆)に専念いただけます。
医薬品の製造販売承認申請から取得までに必要な資料作成をワンストップでご支援してきた「新薬申請サービス」のノウハウを生かしたサービスメニューです。
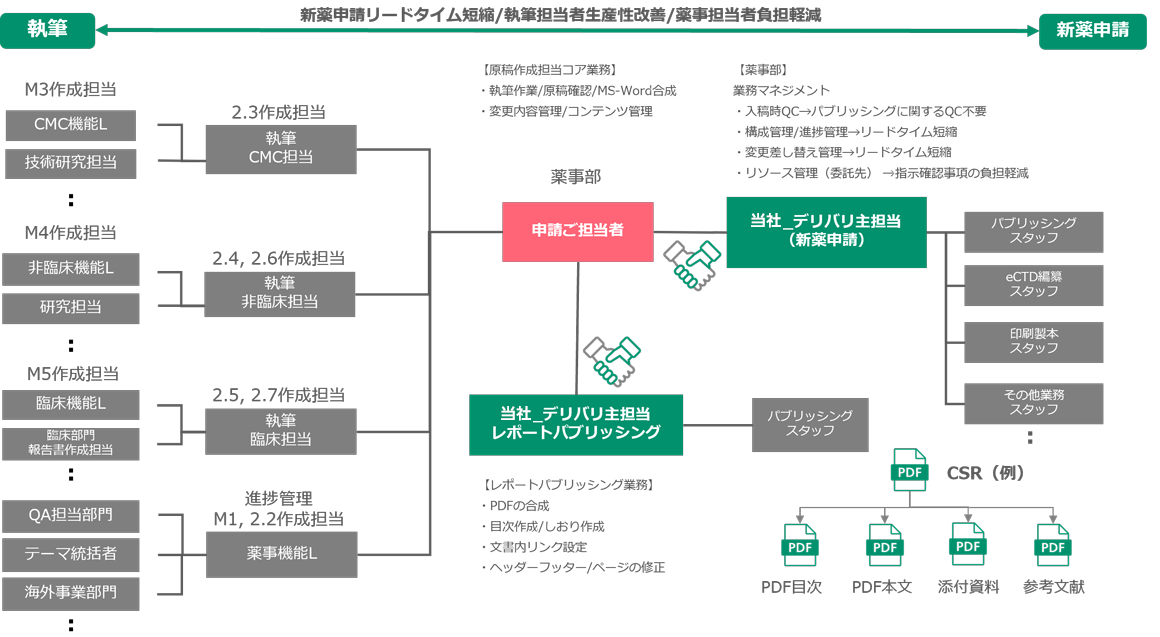
お客様のニーズに合わせ業務設計しておりますが「レポートパブリッシングサービス」の標準メニューをご紹介いたします。
| カテゴリ | 作業内容のイメージ |
|---|---|
| テキストPDFの作成 | Word文書からPDFファイルを作成します。 |
| 紙資料の電子化およびPDF文書の加工 | 紙資料についてはスキャンしてPDF化を行います。 |
| 文書の結合 | リーフPDF(PDF単体)ファイルからCSR1ファイルに結合します。 |
| 目次作成 | リーフPDF(PDF単体)ファイルから目次を作成します。 |
| 文書内しおり作成/点検 | 図表や参照を示す頁へ文書内リンクを作成・点検します。 |
| 文書内リンクの作成/点検 | CSRの項目に合わせた文書内しおりを作成/点検します。 |
| 識別子の付与 | PDFファイルの各ページのヘッダーに、試験名および通しページ番号を付与します。 |
| SR化 | 規制要件に合致したPDFへ最適化を図ります。 |
レポートパブリッシングサービスに関する資料をご用意しました。
下部お問い合わせボタンより資料ダウンロードご希望のサービス名を記載のうえお申し込みください。

コア業務である執筆に専念できる
- 申請資料のコンテンツ作成(執筆)→申請資料の統一性が図れ、品質向上した
- 規制対応→日米欧の3極の通知を熟知した外部のプロに任せるので品質の安定・向上が図れた
申請業務マネジメントが軽減できた
- 各原部署からの入稿対応→パブリッシングに関するQC不要となった
- 各原部署からの文書の変更差し替え管理→リードタイムが短縮できた
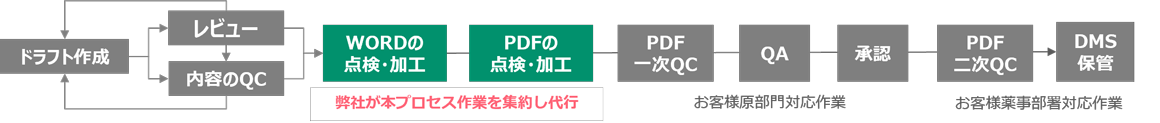
執筆担当が各自で実施しているファイル合成処理および編集編纂オペレーションを当社が丸ごと処理いたします。
- 申請リードタイムの短縮に貢献
- 執筆担当者の生産性改善と薬事担当者の業務軽減を支援
- 業界標準仕様の提供とオフサイト化により業界横断でのリソース(システム+人材)共有を実現
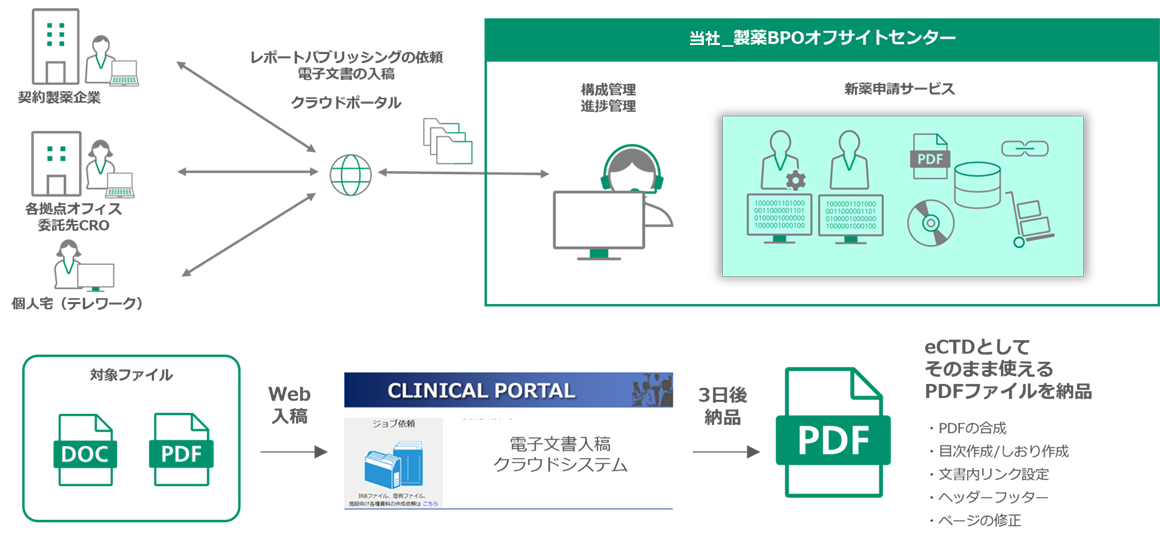
規制要件に合致した社内標準仕様の徹底が図れ、QCD向上に貢献した事例
- 対象業務:サブミッション レポートパブリッシング
- 依頼部署数および原稿入稿担当者数:臨床、非臨床、CMC、その他(約50名から依頼)
- 提供サービス:PDF合成/目次作成/しおり作成/文書内リンク設定/ヘッダー・フッター/頁の修正など
- SLA:薬事部さま主導で取り決めた標準仕様書に基づき、3-10営業日で納品
- ご支援頻度:毎日、約10拠点からのご依頼
| 効果(訂正効果のみ記載) | |
|---|---|
| 品質 |
|
| コスト |
|
| 工数 | 各拠点の研究開発部門に従事している資料作成担当者の次の工数を削減できた
|
| デリバリー |
|



